-
1 概述
-
2 视频
-
3 教案PPT
-
4 习题检测
蒸馏操作是气液两相间的传质过程,气液两相达到平衡状态是传质过程的极限。因此,气液平衡关系是分析精馏原理、解决精馏计算的基础。
(一)两组分理想物系的气液平衡
所谓理想物系是指液相和气相应符合以下条件:
(1)液相为理想溶液,遵循拉乌尔定律;
(2)气相为理想气体,遵循道尔顿分压定律。当总压不太高(一般不高于10000 kPa)时,气相可视为理想气体。
理想物系的相平衡是相平衡关系中最简单的模型。严格地讲,理想溶液并不存在,结构相似、性质极相近的组分组成的物质,如苯-甲苯、甲醇-乙醇、常压及150 oC以下的各种轻烃的混合物,可近似按理想物系处理。
1、气液平衡相图
用相图来表达气液平衡关系较为直观,尤其对两组分蒸馏的气液平衡关系的表达更为方便,影响蒸馏的因素可在相图上直接反映出来。蒸馏中常用的相图为恒压下的温度-组成图及气-液相组成图。
(1)温度-组成图(t-x-y)在恒定的总压下,溶液的平衡温度随组成而变,将平衡温度与液(气)相的组成关系标绘成曲线图,该曲线图即为温度-组成图或t-x-y图。
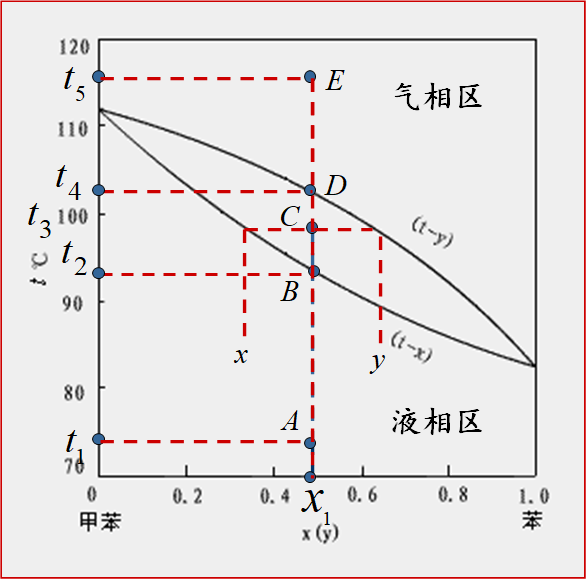
图1-1 苯-甲苯混合液的平衡温度-组成图
图1-1所示为总压101.3kPa下,苯-甲苯混合液的平衡温度-组成图。图中以x(或y)为横坐标,以t为纵坐标。图中有两条曲线,上方的曲线为t-y线,表示混合物的平衡温度t与气相组成y之间的关系,称为饱和蒸气线或露点线;下方的曲线为t-x线,表示混合物的平衡温度t与液相组成x之间的关系,称为饱和液体线或泡点线。上述的两条曲线将t-x-y图分成3个区域,其中饱和液体线以下的区域代表未沸腾的液体,称为液相区;饱和蒸气线上方的区域代表过热蒸气,称为过热蒸气区;两曲线包围的区域表示气液两相同时存在,称为气液共存区。
在恒定的压力下,若将温度为t1、组成为x1(图中点A)的混合液加热,当温度升高到t2(点B)时,溶液开始沸腾,此时产生第一气泡,该温度取了为泡点温度tB。继续升温到t3(点C)时,气液两相共存,其气相组成为y,液相组成为x,两相互为平衡。同样,若将温度为t5、组成为y1(点E)的过热蒸气冷却,当温度降到t4(点D)时,过热蒸气开始冷凝,此时产生第一个液滴,该温度即为露点温度tD。继续降温到t3(点C)时,气液两相共存。
由图1-1可见,气液两相呈平衡时,气液两相的温度相同,但气相组成(易挥发组分)大于液相组成;若气液两相组成相同时,则露点温度总是大于泡点温度。
(2)气-液相组成图(x-y图) x-y图直观地表达了在一定压力下,处于平衡状态的气液两相组成的关系,在蒸馏计算中应用最为普遍。
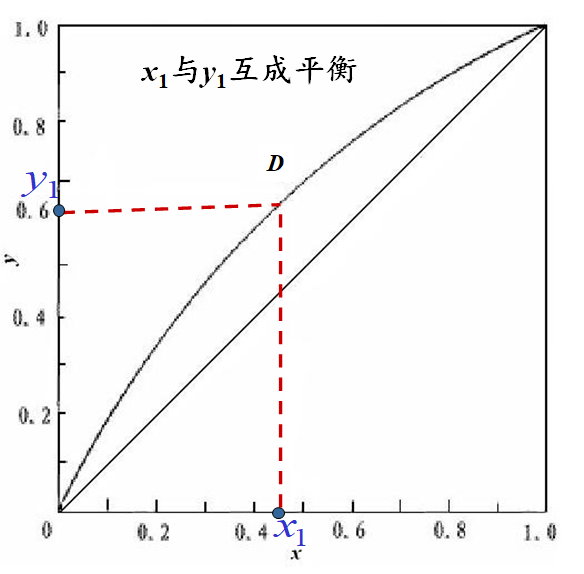
图1-2 苯-甲苯混合物系的x-y图
图1-2所示为总压101kPa下,苯-甲苯混合物系的x-y图。图中以x为横坐标,y为纵坐标。图中的曲线代表液相组成和与之平衡的气相组成间的关系,称为平衡曲线。若已知液相组成x1,可由平衡曲线得出与之平衡的气相组成y1,反之亦然。图中的直线为对角线(y=x),该线作为参考线供计算时使用。对于理想物系,气相组成y恒大于液相组成x,故平衡线位于对角线上方。平衡线偏离对角线愈远,表示该溶液愈易分离。
应予指出,x-y图是在恒定压力下测得的,但实验表明,在总压变化范围为20~30%下,x-y图变动不超过2%。因此,在总压变化不大时,外压对x-y线的影响可忽略。x-y图还可通过t-x-y图作出。常见的两组分物系常压下的平衡数据,可从理化手册中查得。
2、气液平衡的关系式
前已述及,用相图来表达的气液平衡关系较为直观,但在定量计算中采用气液平衡关系式更为方便。
(1)拉乌尔定律实验表明,当理想溶液的气液两相呈平衡时,溶液上方组分的分压与溶液中该组分的摩尔分数成下比,即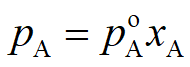 ,
,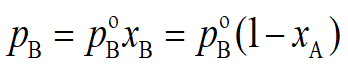 。
。
下标A表示易挥发组分,B表示难挥发组分。
为了简单起见,常略去上式表示相组成的下标,习惯上以x和y分别表示易挥发组分在液相和气相中的摩尔分数,发(1-x)和(1-y)分别表示难挥发组分的摩尔分数。
溶液上方的总压P等于各组分的分压之和,即
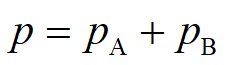 或
或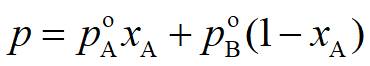
整理上式得到
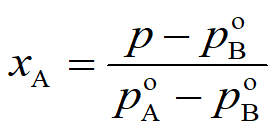
上式表示气液平衡时,液相组成与平衡温度之间的关系,称为泡点方程。根据此式可计算一定压力下,某液体混合物的泡点温度。
(2)以平衡常数表示的气液平衡方程,对拉乌尔定律进行分析,即可得出以平衡常数表示的气液平衡方程。
设平衡的气相遵循道尔顿分压定律,即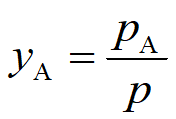 或
或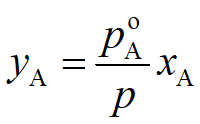 ,代入泡点方程,整理可得:
,代入泡点方程,整理可得: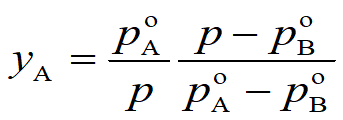 。
。
上式表示气液平衡时气相组成与平衡温度之间的关系,称为露点方程。根据此式可计算一定压力下,某蒸气混合物的露点温度。
若令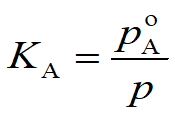 ,则
,则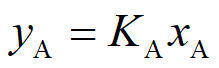 。
。
上式即是以平衡常数表示的气液平衡方程,KA称为气液相平衡常数,简称平衡常数。
(3)以相对挥发度表示的气液平衡方程,前已述及,蒸馏的基本依据是混合液中各组分挥发度的差异。纯组分的挥发度是指液体在一定温度下的饱和蒸气压。而溶液中各组分的挥发度可用它在蒸气中的分压和与之平衡的液相中的摩尔分数之比来表示,即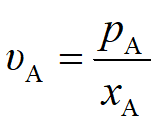 ,
,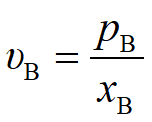
对于理想溶液,因符合拉乌尔定律,则有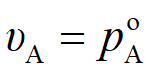 ,
,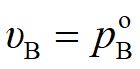
挥发度表示某组分挥发能力的大小,随温度而变,在使用上不太方便,故引出相对挥发度的概念。习惯上将易挥发组分的挥发度与难挥发组分的挥发度之比称为相对挥发度,公式为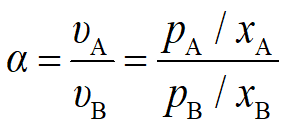 ,略去下标,经整理可得
,略去下标,经整理可得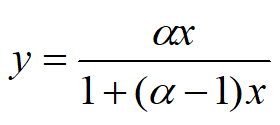
上式即是以相对挥发度表示的气液平衡方程。在蒸馏的分析和计算中,常用上式来表示气液平衡关系。
根据相对挥发度a值的大小可判断某混合液是否能用一般蒸馏方法分离及分离的难易程度。或a>1,表示组分A较B容易挥发,a值偏离1的程度愈大,挥发度差异愈大,分离愈容易。若a=1,由气液平衡方程可知y=x,此时不能用普通的蒸馏方法加以分离,需要采用特殊精馏或其他分离方法。


